JPCA:基于QM/MM的大分子体系能量分解分析方法
Published Time: 2024-07-19 14:14:27
分子间相互作用是现代分子科学研究的关键问题之一,准确分析分子间相互作用对于理解各种物理、化学过程非常重要。能量分解分析(EDA)是一种基于量子化学计算的定量分析方法,构建起了分子相互作用的理论计算与概念解释的桥梁,对我们理解各种化学现象具有很重要的意义。
随着化学、材料、生命科学等学科的快速发展,人们迫切需要精准深入理解和有效调控多尺度复杂分子体系,对EDA方法提出了新的挑战。最近,苏培峰课题组将QM/MM方法与GKS-EDA相结合,提出了GKS-EDA(QM/MM),用于大分子体系的相互作用,工作发表在J. Phys. Chem. A。
GKS-EDA(QM/MM)能量项定义与计算流程
与GKS-EDA相同,GKS-EDA(QM/MM) 同样将相互作用分解为静电、交换排斥、极化、色散相关等项:
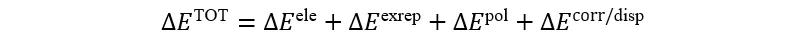
与其他QM/MM EDA方法不同的是,GKS-EDA(QM/MM) 适用于各种QM/MM平台以及各种力场,从而可以灵活的考虑各种溶剂效应对相互作用的影响。当MM部分逐渐趋于零时,GKS-EDA(QM/MM) 应当回归到GKS-EDA结果。
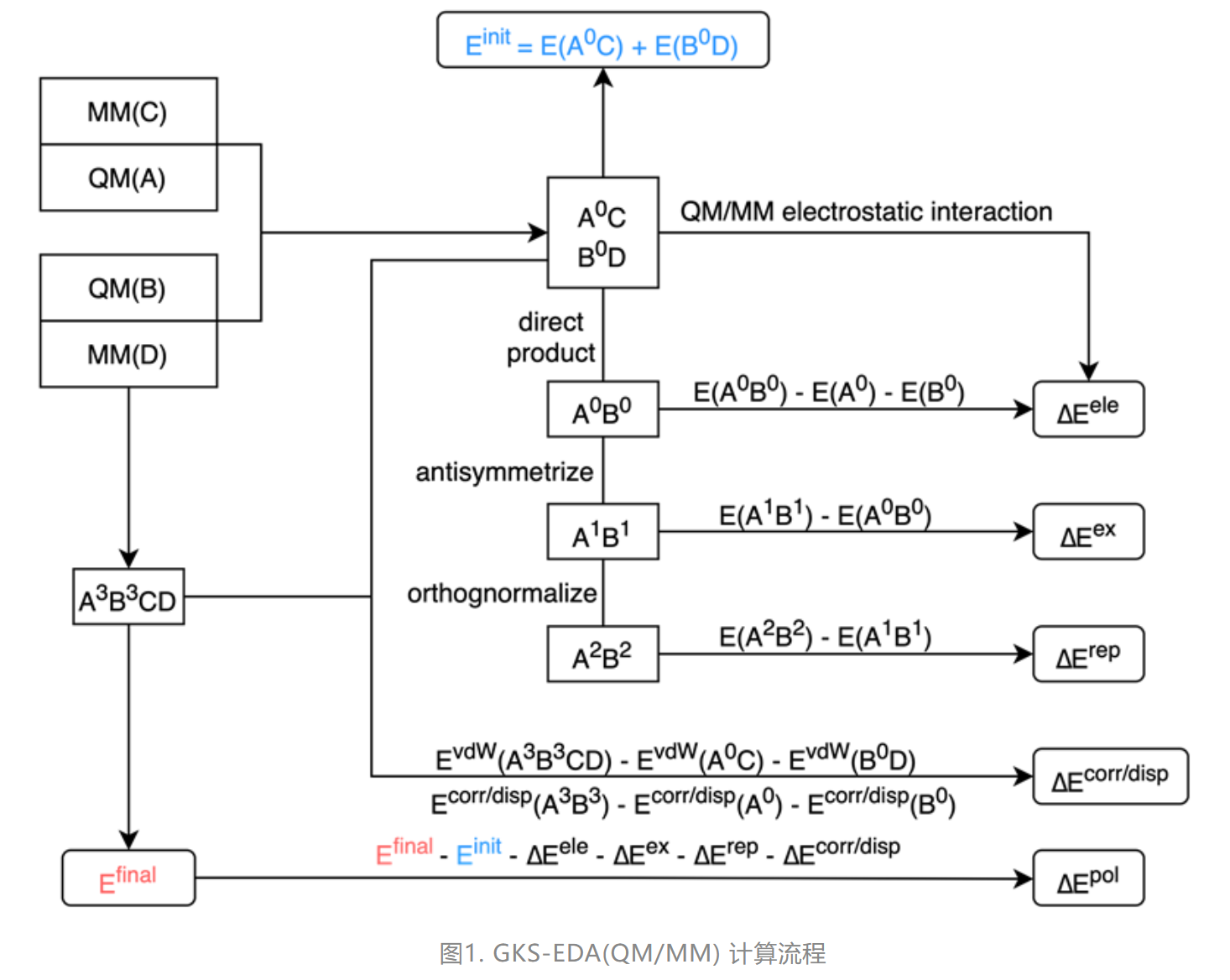
计算流程如图1所示,不失一般性,整个体系被划分为两个单体,且两单体都包含有QM和MM区域。A与B之间的相互作用可直接由GKS-EDA计算,它们的起始波函数均被对应单体的MM环境所极化。QM/MM之间,以及两单体MM之间的相互作用主要包含静电项和色散项,由于不显含电子,两单体MM部分之间没有交换和排斥相互作用。将所有静电项求和得到总的静电相互作用能,相关和所有色散项归并为相关/色散项。考虑到极化项与各种力场密切相关,而且体系划分存在多体效应,极化项并非逐项求和而是由总相互作用能与其他分项作差得到。
GKS-EDA(QM/MM) 用于溶质-溶剂 (H3O+•••water) 相互作用分析化
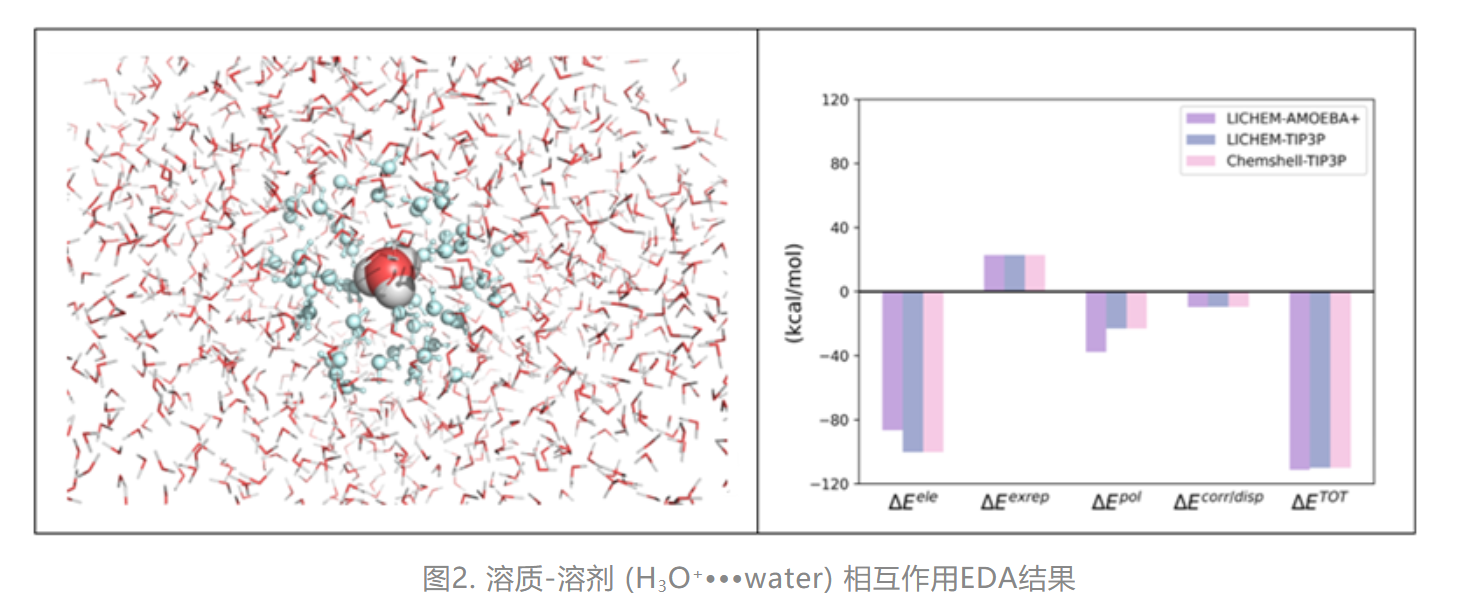
图2展示了GKS-EDA(QM/MM) 计算H3O+与1435个水分子相互作用的结果。H3O+及其周围第一溶剂化层52个水分子用QM描述而其余水分子用力场描述。QM区域中,H3O+为一个单体而第一溶剂化层52个水分子为另一个单体。由右图可看出,由于水力场最为成熟,采用不同QM/MM程序与极化/非极化力场计算的总体相互作用能是相近的,但极化力场给出较大的极化相互作用项,非极化力场则倾向于低估极化作用。因此,GKS-EDA(QM/MM) 可以用于各种MM力场的评估比较。
GKS-EDA(QM/MM) 用于蛋白-配体(MMP13-pyrimidinetrione)相互作用分析
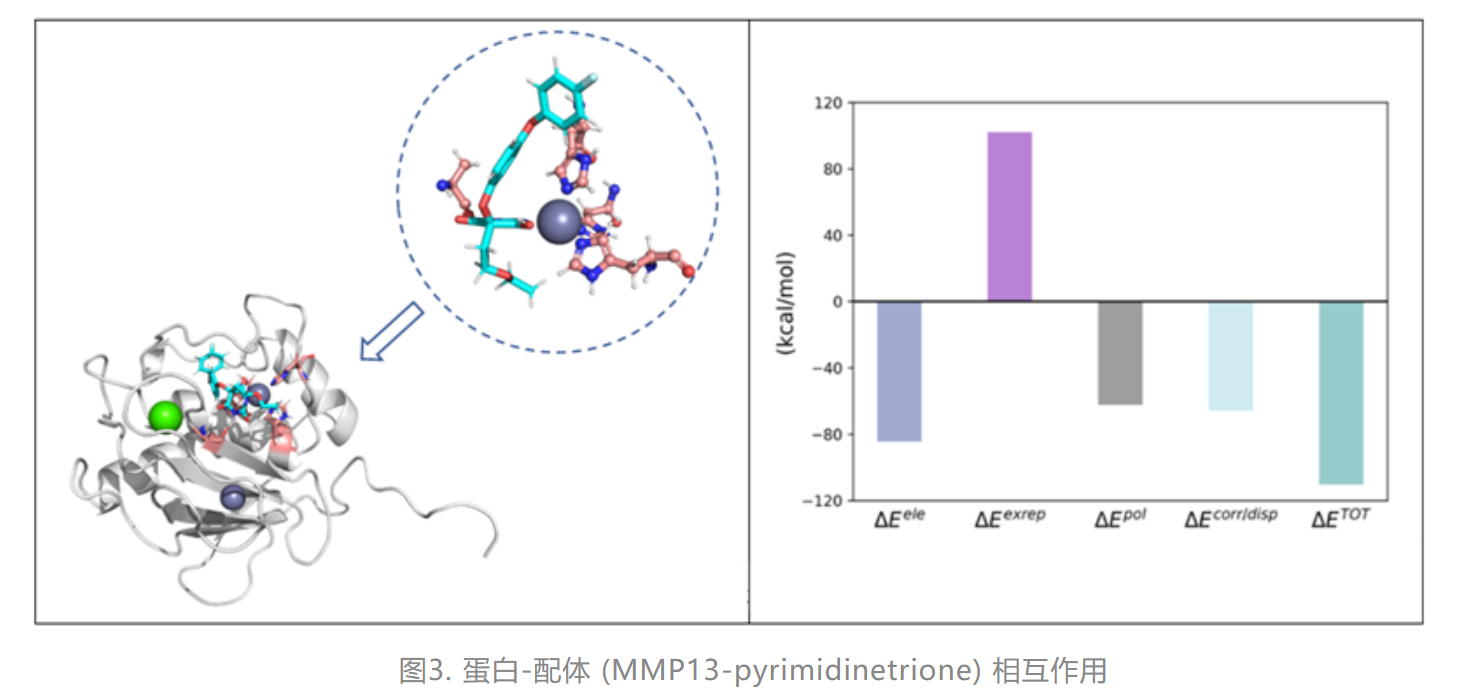
GKS-EDA(QM/MM) 还可以对含Zn2+金属酶活性位点的蛋白质-配体相互作用进行分析。图3给出了蛋白-配体 (MMP13-pyrimidinetrione) 相互作用,虚线标出QM部分,QM区域中,标蓝色的氨基酸残基与Zn2+为一个单体而其余部分为另一个单体。从GKS-EDA(QM/MM) 结果看,该体系中并不存在占主导地位的能量项贡献。静电、极化以及相关/色散都在促进蛋白质与配体的结合中发挥了重要作用。氢键以及Zn2+与含N配体的相互作用决定了静电和极化项(Zn2++在含N配体的作用下极化程度很高)。相关/色散项是来自抑制剂中的疏水环和碳链与附近蛋白质残基之间的多重 vdW 相互作用,以及 QM 模拟的蛋白质残基与配体之间的电子相关贡献。 综上,该方法可以结合不同的QM/MM程序,对溶质-溶剂、蛋白质-配体和蛋白质-蛋白质等复杂体系的相互作用进行分析,为定量理解复杂环境中分子相互作用变化规律提供有用工具。该方法以后将整合在XACS云计算平台上,敬请期待!

论文信息:
QM/MM-Based Energy Decomposition Analysis Method for Large Systems
Xuewei Xiong, Ran Friedman*, Wei Wu, and Peifeng Su*
J. Phys. Chem. A, 2024, 128, 18, 3529–3538
Publication Date: April 30, 2024
DOI:10.1021/acs.jpca.4c00183
© 2024 American Chemical Society